

Questo sito è dedicato a personale sanitario qualificato, coinvolto nella gestione del carcinoma gastrico o della giunzione gastroesofagea.
Questo sito contiene risorse educazionali ed è sviluppato da Astellas Pharma S.p.A.
MAT-IT-NON-2025-00178 Nov 2025






Nonostante un panorama offuscato dalla complessità, i biomarker consolidati ed emergenti stanno ampliando la nostra visione delle popolazioni di pazienti, e i test sui biomarker potrebbero fornire un profilo paziente più completo e portare a decisioni più informate.


Questo elenco di biomarker del tumore gastrico non è esaustivo. Potrebbero esistere altri biomarker non menzionati in questo sito.
CLDN18.2=claudina18.2; FGFR2b=Recettore del fattore di crescita dei fibroblasti 2b; HER2=recettore 2 del fattore di crescita epidermico umano; MSI=instabilità dei microsatelliti; PD-L1=Ligando della proteina 1 della morte cellulare programmata.
UN BISOGNO INSODDISFATTO
Il tasso di sopravvivenza a 5 anni per il tumore gastrico è del 32% in Italia; in Europa è del 25%.1

Nel 2020*, in Italia sono stati diagnosticati oltre 14.500 nuovi casi di carcinoma allo stomaco, è il sesto carcinoma per incidenza in Italia.1

Nel 2020, vi sono stati oltre 95.000 decessi in Europa a causa di tumore gastrico, che si trova al 6° posto per tasso di mortalità tra i tumori in Europa.2


Nel 2020*, vi sono stati 8.700 decessi in Italia a causa di tumore gastrico, che si trova al 4° posto per tasso di mortalità tra i tumori in Italia.1
Nel 2020, vi sono stati oltre 768.000 decessi nel mondo dovuti a tumore gastrico, ponendolo al 4° posto per tasso di mortalità tra i tumori a livello mondiale.3


Scopri di più sui test dei biomarker in questo video con il Dottor Daniel Swinson, consulente oncologo medico presso gli ospedali universitari di Leeds e il Professor Nicholas West, consulente istopatologo presso gli ospedali universitari di Leeds. Il video esplora lo scenario ideale per il test dei biomarker e spiega perché ciò potrebbe non sempre verificarsi nella pratica clinica 'real-world '. Il dottor Swinson descrive inoltre come ottimizzare i test sui biomarker per accelerare le decisioni terapeutiche.
aiutano a identificare sottogruppi precedentemente non definiti di pazienti affetti da tumore mG/GEJ:
BIOMARKER CONSOLIDATI
sono utilizzati per fornire informazioni di supporto alle decisioni cliniche:
La maggior parte dei biomarker emergenti e consolidati può essere rilevata utilizzando test standard ampiamente accettati come l’IHC
BIOMARKER EMERGENTI
CLDN18.2:
IHC13*
FGFR2b:
IHC, NGS14,15*†
BIOMARKER CONSOLIDATI
PD-L1:
IHC16–19*‡
HER2:
IHC, ISH, NGS16–19*§
MSI/MMRd:
PCR, NGS/IHC16–18*
IHC=immunoistochimica; ctDNA=DNA tumorale circolante; ISH=ibridazione in situ; MMR=processo di riparazione mismatch; NGS=sequenziamento next generation; PCR=reazione a catena della polimerasi.
*L'espressione utilizza test IHC e PCR;13,16–18 l'amplificazione utilizza test ctDNA, ISH e NGS.15–19
† L'IHC rileva la sovraespressione di FGFR2b; NGS rileva l'amplificazione del gene FGFR2 da parte del ctDNA.15,16
‡ Vari test diagnostici.20
§ Altri metodi ISH (FISH=ISH fluorescente; SISH=ISH con argento; CISH=ISH cromogenico; DDISH=ISH bicolore con doppio aptene).19
I biomarker emergenti sono altamente prevalenti tra i biomarker utilizzati per i tumori mG/GEJ.
Di seguito sono riportate le stime sulla prevalenza dei biomarker tratte da studi selezionati. I dati sulla prevalenza possono variare tra gli studi a causa dell’eterogeneità del tumore, delle differenze nella popolazione di pazienti, della metodologia della sperimentazione clinica e dei test diagnostici utilizzati.10,21-23
BIOMARKER EMERGENTI
CLDN18.213,21,24
(espressione elevata)‖¶
33–38%
FGFR2b22
(positività)
30%
‖ Colorazione 2+/3+ mediante IHC nel ≥70% delle cellule tumorali. Include l'adenocarcinoma localmente avanzato non resecabile o metastatico (mG/GEJ).13
¶ Espressione elevata: colorazione IHC 2+/3+ nel ≥75% delle cellule tumorali.21
TASSI DI PREVALENZA GLOBALE DEI BIOMARKER CONSOLIDATI
PD-L123,25
(VariabIle a causa di molteplici fattori)**
CPS ≥1: 67-73%
CPS ≥5: 29-31%
CPS ≥10: 16-18%
HER2
(Positività)
22%10
MSI
(MSI-elevata)
4-6%26
CPS=score positivo combinato; mG/GEJ=tumore gastrico/della giunzione gastro-esofagea metastatico.
**La prevalenza di PD-L1 a varie soglie di CPS è ancora in fase di studio. I dati provengono da uno studio randomizzato e controllato e da uno studio retrospettivo di cartelle cliniche 'real-world '.23,25
Cronologia delle scoperte di biomarker targetizzabili27–31


Nel 2021, ASCO ha riconosciuto la profilazione molecolare nel tumore gastrointestinale come 'Advance of the Year' (progresso più rilevante dell'anno).32
Il professor Nicholas West descrive le considerazioni chiave dal punto di vista tecnico e del personale quando si implementa un nuovo test sui biomarker nella pratica di routine, e condivide alcune delle sue raccomandazioni e delle sue esperienze di apprendimento.
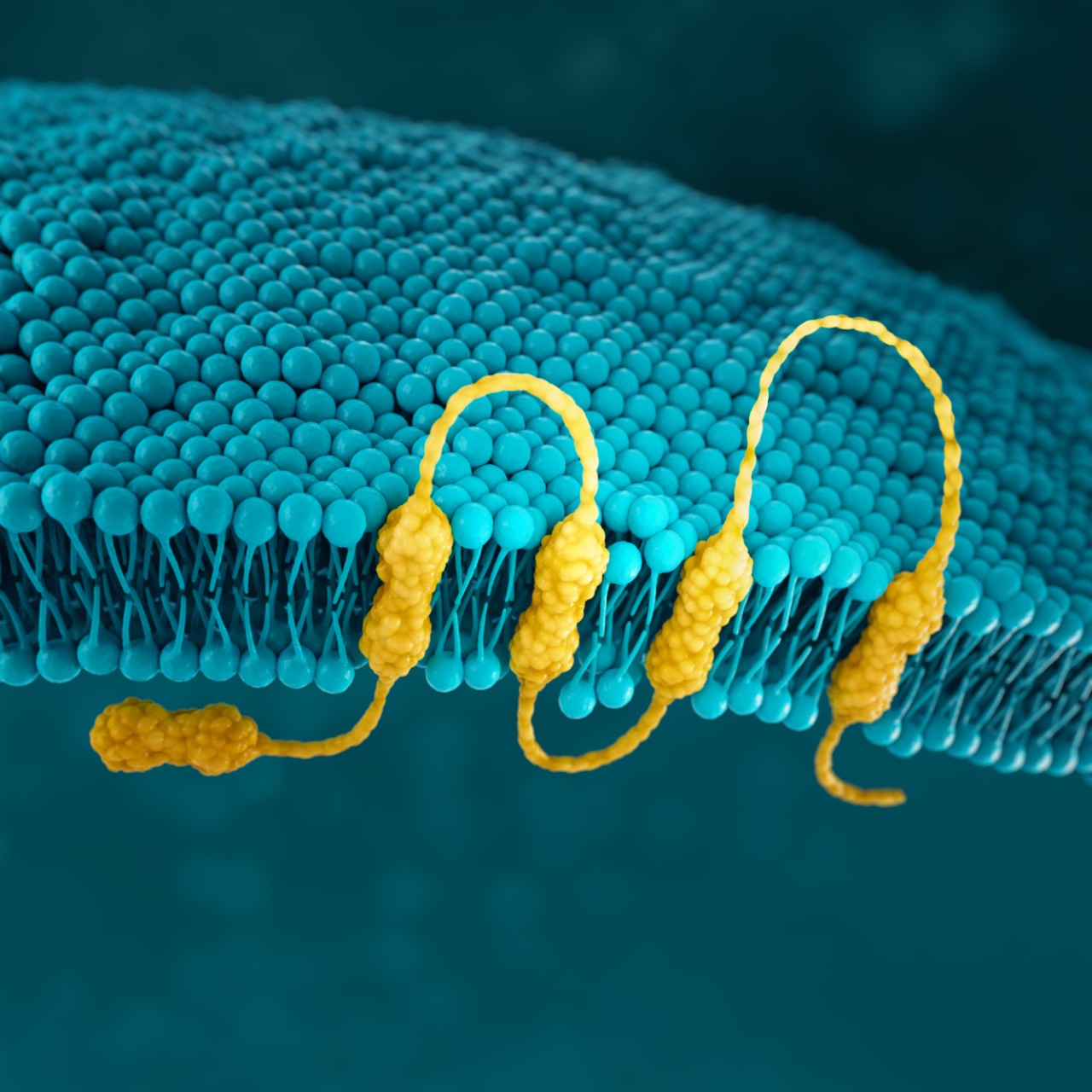
CLDN18.2
Le claudine sono una famiglia di proteine transmembrana:4,30
Le claudine sono una componente importante delle giunzioni strette epiteliali ed endoteliali, che sono coinvolte nel controllo del flusso di molecole tra le cellule.4–6
Le claudine sono presenti in tutto il corpo, ma due specifiche isoforme di splicing di CLDN18 sono localizzate in alcuni tipi di tessuti.4,30
Studi preclinici hanno dimostrato che CLDN18.2 può diventare più esposta e accessibile agli anticorpi con lo sviluppo di sviluppo di tumore gastrico.4,34,35
CONFINATA NEI TESSUTI SANI
Nelle cellule epiteliali gastriche, CLDN18.2 è generalmente nascosta nel complesso sopramolecolare delle giunzioni strette.4,6,35
La sua funzione è la regolazione delle proprietà della barriera selettiva, e contribuisce all'adesione epiteliale cellula-cellula.4–7
ESPOSTA IN FASE DI CANCEROGENESI


La trasformazione maligna porta a interruzioni della polarità e perdita di struttura.34,35
Di conseguenza, CLDN18.2 potrebbe essere più esposta e accessibile agli anticorpi.4,34,35
MANTENUTA DURANTE LA TRASFORMAZIONE


La presenza di CLDN18.2 viene mantenuta durante tutta la trasformazione maligna, sia nel sito del tumore primario che nella malattia metastatica.4,34
Sebbene non sia presente nei tessuti sani oltre alle cellule epiteliali gastriche, CLDN18.2 può attivarsi anche nei tumori esofagei, pancreatici, polmonari e ovarici.4
Mentre circa il 70% dei tumori G/GEJ localmente avanzati e metastatici esprime CLDN18.2 (a qualsiasi livello), studi recenti hanno dimostrato che circa il 38% dei pazienti con mG/GEJ sono CLDN18.2 positivi (espressione elevata).21,24


Pochi pazienti con tumore G/GEJ localmente avanzato o metastatico e positivi a CLDN18.2 (alta espressione*) risultano positivi anche per altri biomarker.21
Nel valutare la relazione tra CLDN18.2 e altri biomarker, i dati attuali suggeriscono una sovrapposizione limitata.








* Espressione elevata di CLDN18.2: intensità 2+ e 3+ in ≥75% delle cellule tumorali.20
† La popolazione dello studio era limitata a 350 pazienti caucasici con carcinoma G/GEJ metastatico, di cui 117 soggetti con espressione elevata di CLDN18.2. FGFR2b non è stato valutato in questo studio.
CLDN18.2 è espressa sia nei tumori di tipo diffuso che nei tumori di tipo intestinale.6

FGFR2b
FGFR2b è un recettore tirosin chinasico che ha un ruolo nel normale sviluppo cellulare38
L'amplificazione di FGFR2 è significativamente associata alla sovraespressione del recettore FGFR2 nel tumore gastrico41
CELLULA NORMALE
Nelle cellule normali, la segnalazione FGFR è una componente essenziale per lo sviluppo cellulare. La via deregolamentata dell'FGFR2, attraverso mutazioni o traslocazioni, svolge un ruolo fondamentale in diversi tipi di tumore.42
CELLULA DI TUMORE GASTRICO
La sovraespressione di FGFR2 e la segnalazione sovraregolata possono essere eventi chiave in un sottotipo di tumore gastrico. Il rilevamento dell’amplificazione di FGFR2 è stato il fondamento del pre-screening dei pazienti per la sovraespressione del recettore FGFR2.42
Il rilevamento di isoforme specifiche di FGFR2 (ad esempio FGFR2b) o di sovraespressione del ligando FGF possono rappresentare dei biomarker predittivi di tumore gastrico innovativi e maggiormente informativi.42
La positività a FGFR2b può essere osservata nel 30% dei tumori mG/GEJ.22


Positività FGFR2b: sovraespressione (IHC) e/o amplificazione genica mediante ctDNA (NGS).
Il rilevamento di FGFR2b può essere effettuato con i seguenti test:15,16
FGFR2b è un biomarker relativamente nuovo nel tumore gastrico e, pertanto, sono disponibili dati limitati riguardo alla sua sovrapposizione nell'espressione con altri biomarker
| Biomarker | Biomarker | Prevalenza di sovrapposizione | Riferimento |
|---|---|---|---|
| FGFR2b | CLDN18.2 | Non nota* | Attualmente non disponibile* |
| FGFR2b | PD-L1+ | Non nota† | Attualmente non disponibile† |
| FGFR2 | HER2 (3+) | 0.3% | Su 201443 |
| FGFR2b | MSI/MMR | Non nota‡ | Attualmente non disponibile‡ |
* Una ricerca su PubMed utilizzando i termini di ricerca (gastric cancer) AND (FGFR2) AND (CLDN18.2) non ha individuato alcuna pubblicazione.
† Una ricerca su PubMed utilizzando i termini di ricerca (gastric cancer) AND (FGFR2) AND (PD-L1) ha individuato cinque articoli, nessuno dei quali includeva informazioni relative alla sovrapposizione di prevalenza di questi due biomarker.
‡ Una ricerca su PubMed utilizzando i termini di ricerca (gastric cancer) AND (FGFR2) AND (MSI) ha individuato sette articoli, nessuno dei quali includeva informazioni relative alla sovrapposizione di prevalenza di questi due biomarker. Una ricerca utilizzando i termini di ricerca (gastric cancer) AND (FGFR2) AND (MMR) ha individuato due articoli, nessuno dei quali includeva informazioni relative alla sovrapposizione di prevalenza di questi due biomarker.
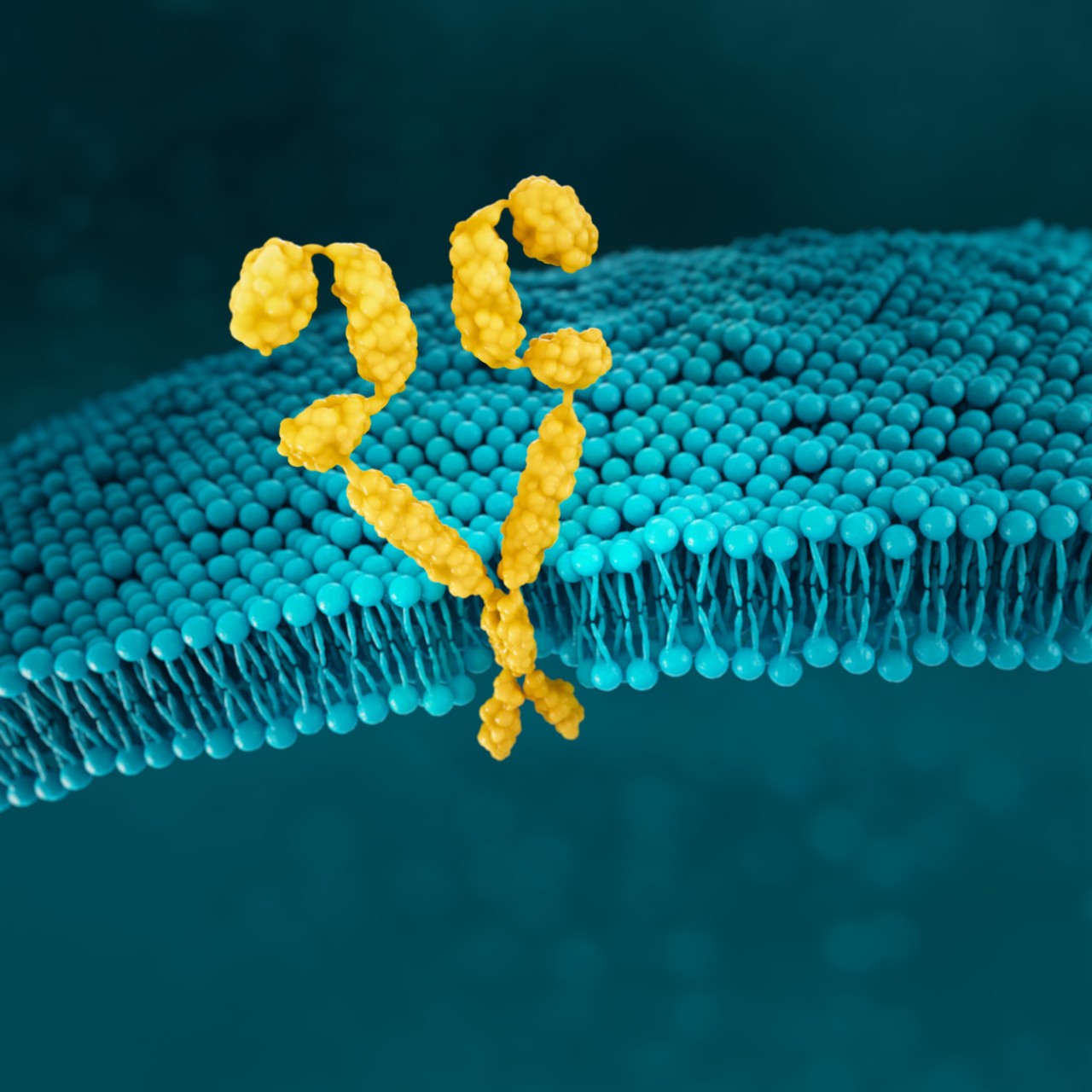
HER2
HER2 è un recettore tirosin chinasico che è sovraespresso e/o amplificato nei tumori G/GEJ metastatici.8
HER2 è un proto-oncogene coinvolto nelle vie di segnalazione che portano alla crescita e alla differenziazione cellulare.19
Nelle cellule normali, sulla superficie cellulare esistono pochi recettori HER2 (vedi figura sotto), quindi si formano pochi eterodimeri e i segnali di crescita sono relativamente deboli e controllabili45
CELLULA NORMALE
Cellula sana con bassa espressione di recettori della proteina HER2 e pochi eterodimeri del recettore HER2 sulla superficie cellulare.45
CELLULA TUMORALE HER2+
HER2 è sovraespresso e/o amplificato, sulla superficie cellulare si formano numerosi eterodimeri del recettore
HER2 e la segnalazione cellulare viene potenziata.45
Quando HER2 è sovraespresso, si formano più recettori proteici HER2 e la segnalazione cellulare è più forte, il che si traduce in una maggiore reattività ai fattori di crescita e alla proliferazione maligna.45
La positività a HER2 è stata segnalata nel 22% dei tumori G/GEJ avanzati.10


Positività HER2: sovraespressione (IHC3+) e/o amplificazione genica (FISH-positivo).
Il rilevamento di HER2 può essere effettuato con metodi IHC, ISH e NGS e in genere è maggiormente associato a tumori di tipo intestinale.10,16,19*
Esiste una sovrapposizione limitata tra HER2 e altri biomarker di tumore gastrico, con tre studi che riportano una sovrapposizione minima tra HER2 e CLDN18.2
| Biomarker | Biomarker | Prevalenza di sovrapposizione | Riferimento |
|---|---|---|---|
| HER2 | CLDN18.2 | 12-15% | Pellino 2021,21 Moran2018,46 Schuler 201747 |
| HER2 | PD-L1+ | 7,4% | Angell 201848 |
| HER2 | MSI | 11,1% | Angell 201848 |
| HER2 | FGFR2 | 0,3% | Su 201443 |
CISH=ISH cromogenico; DDISH=ISH bicolore doppio aptene; FISH=ISH fluorescente; IHC=immunoistochimica; ISH=ibridazione in situ; NGS=sequenziamento next generation; SISH=ISH con argento.
*Il test IHC/ISH deve essere preso in considerazione per primo, seguito da ulteriori test NGS, a seconda dei casi.16
MSI
L'espressione di MSI è associata all'instabilità genomica e ad una maggiore suscettibilità allo sviluppo del tumore.8
I microsatelliti sono sequenze ripetute di nucleotidi nel DNA.8
I principali meccanismi attraverso i quali si verifica il fallimento del sistema MMR sono dovuti a cambiamenti genetici ed epigenetici in h-MLH1 e h-MSH2 e, meno frequentemente, in h-MSH6 e h-PMS250
TUMORE CON STABILITÀ MICROSATELLITARE
TUMORE CON MSI ELEVATO
MMRd=deficit di MMR.
Poiché le mutazioni somatiche nei tumori gastrici MSI sono comuni, è difficile individuare i geni bersaglio in cui le mutazioni portano alla carcinogenesi gastrica MSI, tuttavia, i tumori MSI sono più inclini a presentare mutazioni negli oncogeni EGFR, KRAS, PIK3CA e MLK3.50
Nei tumori genomicamente stabili, con un sistema MMRd funzionale, gli errori di replicazione del DNA si verificano raramente. Al contrario, in presenza di livelli di MSI/MMRd elevati, gli errori di replicazione del DNA non vengono né rilevati né riparati, portando a un tumore con un elevato carico mutazionale. Tali cellule tumorali ipermutate producono un eccesso di neoantigeni associati alla mutazione, che vengono presentati dalle molecole MHC sulla superficie cellulare per stimolare l'attivazione dei linfociti T e l'infiltrazione tumorale da parte delle cellule immunitarie. Per contrastare questa vigorosa risposta immunitaria, le cellule tumorali espongono molecole checkpoint, ad esempio PD-L1, per inibire l'attività antitumorale.51,52
PD-L1=ligando della proteina 1 della morte cellulare programmata.
MSI-H è stata segnalata nel 4% dei tumori G/GEJ metastatici.26


MSI-H=MSI-elevata.
Il rilevamento di MSI viene generalmente effettuato con varie metodiche.16
MMRd=deficit di MMR.
Esiste una sovrapposizione variabile tra MSI/MMR e altri biomarker del tumore gastrico; la sovrapposizione tra deficit di MMR (dMMR) e CLDN18.2 è minima
| Biomarker | Biomarker | Prevalenza di sovrapposizione | Riferimento |
|---|---|---|---|
| dMMR | CLDN18.2 | 15% | Pellino 202121 |
| MSI | PD-L1+ | 53,2% | Angell 201848 |
| MSI | HER2 (3+) | 4,2% | Angell 201848 |
| MSI/MMR | FGFR2b | Non nota* | Attualmente non disponibile* |
* Una ricerca su PubMed utilizzando i termini di ricerca (gastric cancer) AND (FGFR2) AND (CLDN18.2) ha individuato sette articoli, nessuno dei quali includeva informazioni relative alla sovrapposizione di prevalenza di questi due biomarker. Una ricerca con i termini (gastric cancer) AND (FGFR2) AND (MMRdI) ha individuato due articoli, nessuno dei quali includeva informazioni relative alla sovrapposizione di prevalenza di questi due biomarker.

PD-L1
PD-L1 è una proteina transmembrana che può essere espressa su varie cellule tumorali e/o cellule immunitarie.53
Trattandosi del regolatore chiave della tolleranza immunitaria e dell’esaurimento immunitario, l’espressione di PD-1 è strettamente controllata:55
CELLULA NORMALE
Nei tessuti normali, il legame PD-1/PD-L1 previene una risposta immunitaria eccessiva e protegge i tessuti dai danni attraverso l’induzione della tolleranza immunitaria.55
CELLULA DI TUMORE GASTRICO
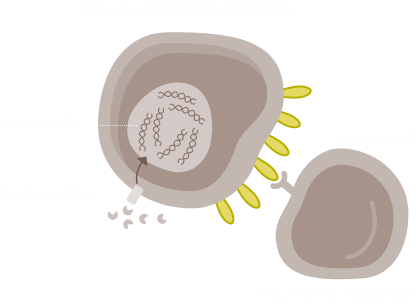
Nel tumore gastrico, l'amplificazione focale del CD274 e la segnalazione mediata dall'IFN-γ possono portare alla sovraespressione di PD-L1 e all'esaurimento funzionale dei linfociti T (linfociti T esausti).55,56
* Il tumore gastrico EBV+ è un sottotipo distinto di tumore gastrico caratterizzato dall’infezione da EBV.
La prevalenza di PD-L1 è stata segnalata per diverse soglie di positività nel corso degli studi clinici23,25*†






CPS=score positivo combinato.
* La popolazione dello studio era limitata a 592 pazienti con tumore G/GEJ localmente avanzato o metastatico che avevano manifestato progressione di malattia dopo la terapia di prima linea con un farmaco a base di platino e fluoropirimidina.25
† Lo studio ha analizzato 56 campioni di biopsie effettuate su pazienti naïve alla terapia di nazionalità tedesca con adenocarcinoma gastrico principalmente non metastatico.23
L'espressione di PD-L1 viene rilevata tramite IHC.16
Quando si valuta la relazione tra PD-L1 a due soglie di positività, i dati suggeriscono che esiste una sovrapposizione limitata con CLDN18.2 e HER2, con una maggiore sovrapposizione con HER2
| Biomarker | Biomarker | Prevalenza di sovrapposizione | Riferimento |
|---|---|---|---|
| PD-L1 (CPS ≥1) | CLDN18.2 | 28% | Pellino 202121 |
| PD-L1 (CPS ≥5) | CLDN18.2 | 20% | Pellino 202121 |
| PD-L1+ | HER2 (3+) | 3,2% | Angell 201848 |
| PD-L1+ | MSI | 53,2% | Angell 201848 |
| PD-L1 | FGFR2 | Non nota* | Attualmente non disponibile* |
* Una ricerca su PubMed utilizzando i termini di ricerca (gastric cancer) AND (FGFR2) AND (PD-L1) ha individuato cinque articoli, nessuno dei quali includeva informazioni relative alla sovrapposizione di prevalenza di questi due biomarker.
SOMMARIO
Scopri i ruoli individuali del patologo e dell'oncologo nel processo di test dei biomarker nel tumore gastrico. Nei prossimi video, il professor Nicholas West e il dottor Daniel Swinson condividono approfondimenti sul loro ruolo nella diagnosi, nell'analisi dei biomarker e nel processo decisionale relativo al trattamento dei tumori gastrici. Nell'ultimo video, i nostri esperti illustrano le interazioni tra oncologi e patologi nella loro pratica attuale e spiegano quali, secondo loro, dovrebbero essere le modalità ideali.
Linee guida
Le linee guida dell'European Society for Medical Oncology (ESMO) sulla diagnosi e il trattamento dei tumori gastrici raccomandano lo screening per HER2, PD-L1 e MSI-H/dMMR, CLDN18.2.17,18
CLDN18.2 è un nuovo biomarker predittivo per l'adenocarcinoma gastrico non resecabile o metastatico localmente avanzato, ma richiede ancora la validazione come metodica di valutazione in un test immunoistochimico (IHC) standardizzato per la pratica clinica.55,56
L'amplificazione/sovraespressione di FGFR2 è in fase di studio e si attende la sua validazione come biomarker predittivo in studi randomizzati e controllati (RCT).55,56
I test dei biomarker sono sempre più informativi sui tumori G/GEJ metastatici man mano che vengono scoperti nuovi indicatori:
* Le metodiche IHC/ISH vanno prese in considerazione per prime, seguite da ulteriori test NGS a seconda dei casi.16
La continua ricerca sui biomarker amplia la nostra visione della popolazione di pazienti, permette di ottenere nuovi dati sui tumori G/GEJ metastatici che potrebbero contribuire a decisioni cliniche più informate.
REFERENCES